신주배정기준일 현재 주주명부에 등재된 주주에 대하여 신주를 배정하며 신주 배정비율이 1:1
신주배정기준일인 8.25일이므로 이날로부터 2일전까지(결제까지 시간소요) 주식을 보유하게 되면 무상증자 가능 무증 주식은 9월 13일에 상장
| 1. 신주의 종류와 수 | 보통주식 (주) | 11,095,233 |
| 기타주식 (주) | - | |
| 2. 1주당 액면가액 (원) | 500 | |
| 3. 증자전 발행주식총수 | 보통주식 (주) | 11,095,233 |
| 기타주식 (주) | - | |
| 4. 신주배정기준일 | 2021년 08월 25일 | |
| 5. 1주당 신주배정 주식수 | 보통주식 (주) | 1 |
| 기타주식 (주) | - | |
| 6. 신주의 배당기산일 | 2021년 01월 01일 | |
| 7. 신주권교부예정일 | - | |
| 8. 신주의 상장 예정일 | 2021년 09월 13일 | |
| 9. 이사회결의일(결정일) | 2021년 08월 09일 | |
| - 사외이사 참석여부 | 참석(명) | 1 |
| 불참(명) | - | |
| - 감사(감사위원)참석 여부 | 참석 | |
10. 기타 투자판단에 참고할 사항
1) 무상증자 배정내역
| 구 분 | 무상증자 전 | 무상증자 배정내역 | 무상증자 후 |
| 보통주 | 11,095,233 | 11,095,233 | 22,190,466 |
| 합 계 | 11,095,233 | 11,095,233 | 22,190,466 |
2) 신주배정 및 단수주 처리 : 상기 신주배정기준일 현재 주주명부에 등재된 주주에 대하여 신주를 배정하며 신주 배정비율이 1:1이므로 단수주는 발생하지 않습니다.
3) 신주의 재원 : 주식발행초과금(5,547,616,500원)
압타바이오 93,500 전일대비 하락 2,700 (-2.81%)

2021.08.10. 장마감
- 전일종가96,200
- 고가98,600
- 저가92,700
- 거래량559,829
- 외국인소진율3.61%
- 시가 총액1조 374억
어제 (8.9. ) 무상증자 소식과 함께 급등했다가 금일은 소폭 조정됨
[압타바이오 플랫폼 기술과 파이프라인 현황]
| 플랫폼 기술 | NOX 기술 | Apta-DC 기술 |
| 작용기전 | NOX저해를 통한 산화성 스트레스 조절로 염증 및 섬유화 억제 | Nucleolin 과발현 암세포 타겟 |
| 질환군 | 당뇨합병증, 항바이러스, 면역항암제개발 (당뇨병성 신증, COVID-19, NASH, 망막병증, 황반변성, 동맥경화, 뇌질환치료제, 면역항암제 개발) |
난치성 항암제 개발 (혈액암, 췌장암, 방광암, 간암) |
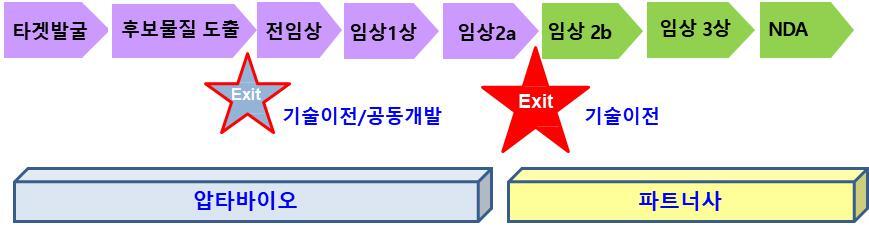
파이프라인 라이센스 아웃 또는 플랫폼 기술의 실시권 부여를 통한 전략적 제휴입니다. 독자적인 플랫폼 기술 및 각 파이프라인에 대한 지식재산권을 확보하였고 이를 기반으로 플랫폼 기술과 질환별 파이프라인 각각에 대한 사업화를 진행
매출실적
(단위: 천원)
| 매출유형 | 품 목 | 2021년 | 2020년 | 2019년 | ||||
| (제13기 1분기) | (제12기) | (제11기) | ||||||
| 수량 | 금액 | 수량 | 금액 | 수량 | 금액 | |||
| 용역매출 | 기술이전 | 수 출 | - | - | - | - | - | - |
| 내 수 | - | - | - | 188,000 | - | 412,000 | ||
| 소 계 | - | - | - | 188,000 | - | 412,000 | ||
| 시약판매 | 유전자 전달체 외 |
수 출 | - | - | - | - | - | - |
| 내 수 | - | 106,435 | - | 153,044 | - | 606,572 | ||
| 소 계 | - | 106,435 | - | 153,044 | - | 606,572 | ||
| 합 계 | 수 출 | - | - | - | - | - | - | |
| 내 수 | - | 106,435 | - | 341,044 | - | 1,018,572 | ||
| 합 계 | - | 106,435 | - | 341,044 | - | 1,018,572 | ||
| <연구개발 진행 총괄표> |
| 구분 | 품목 | 적응증 | 연구시작년도 | 현재진행단계 | 비고 |
| 합성신약 | APX-115 | 당뇨병성 신증 | 2013년 | 임상2상 진행 | 2020년 유럽 임상2상 진입 2021년 유럽 임상2상 완료 예정 |
| COVID-19 | 2020년 | 임상2상 진행 | 2021년 미국 임상2상 진입 | ||
| APX-311 | 비알코올성 지방간염 (NASH) |
2015년 | 임상1상 완료 | 2021년 임상2상 진입 예정 | |
| APX-1004F | 황반변성 (wet-AMD) |
2015년 | 임상1상 신청 | 2018년 삼진제약에 라이선스 아웃 2021년 임상1상 진입 예정 |
|
| APX-1004 | 당뇨성 망막병증 | 2015년 | 비임상 예정 | 2022년 임상2상 진입예정 | |
| APX-5278 | 동맥경화증 | 2014년 | 비임상 예정 | 2021년 비임상 진입예정 | |
| APX-NEW | 뇌질환치료제 | 2019년 | 후보물질탐색 및 효능평가 | 2019년 신규파이프라인 추가 | |
| 면역항암제 | 2019년 | 후보물질탐색 및 효능평가 | 2020년 신규파이프라인 추가 | ||
| Apta-16 | 혈액암 | 2015년 | 임상1/2상 진행 | 2016년 삼진제약에 라이선스 아웃 2021년 임상1/2상 진행 |
|
| Apta-12 | 췌장암 | 2009년 | 비임상 예정 | 2016년 호프바이오사이언스에 라이선스 아웃 | |
| Apta-NEW | 간암 | 2019년 | 후보물질탐색 및 효능평가 | 2019년 신규파이프라인 추가 |
| (기준일 : | 2021년 03월 31일 | ) | (단위 : 주, %) |
성 명관 계주식의종류소유주식수 및 지분율비고기 초기 말주식수지분율주식수지분율
| 이수진 | 본인(대표이사) | 보통주 | 2,400,000 | 21.63 | 2,400,000 | 21.63 | - |
| 문성환 | 등기임원(사장) | 보통주 | 1,200,000 | 10.82 | 1,200,000 | 10.82 | - |
| 문호상 | 배우자 | 보통주 | 120,000 | 1.08 | 120,000 | 1.08 | - |
| 정준희 | 미등기임원 | 보통주 | 13,550 | 0.12 | 13,550 | 0.12 | - |
| 계 | 보통주 | 3,733,550 | 33.65 | 3,733,550 | 33.65 | - | |
| - | - | - | - | - | - | ||
주식 소유현황
| (기준일 : | 2021년 03월 31일 | ) | (단위 : 주) |
구분주주명소유주식수지분율비고
| 5% 이상 주주 | 이수진 | 2,400,000 | 21.63 | 최대주주 |
| 문성환 | 1,200,000 | 10.82 | 등기임원 | |
| - | - | - | - | |
| 우리사주조합 | 43,733 | 0.39 | ||
소액주주비중이 60%이상으로 많은 편
- 코로나-19 경구용 치료제 미국 FDA 임상2상
| 제목 | COVID-19 치료제 APX-115의 US FDA 2상 임상시험 IND 승인 | |
| 2. 주요내용 | ※투자유의사항 임상시험 약물이 의약품으로 최종 허가받을 확률은 통계적으로 약 10% 수준으로 알려져 있습니다. 임상시험 및 품목허가 과정에서 기대에 상응하지 못하는 결과가 나올 수 있으며, 이에 따라 당사가 상업화 계획을 변경하거나 포기할 수 있는 가능성도 상존합니다. 투자자는 수시공시 및 사업보고서 등을 통해 공시된 투자 위험을 종합적으로 고려하여 신중히 투자하시기 바랍니다 1) 임상시험 제목 : - A Phase 2, Double-blind, Placebo-controlled, Efficacy, and Safety Study of APX-115 in Hospitalized Patients with Confirmed Mild to Moderate COVID 19 - 경증에서 중등도 COVID 19가 확인 된 입원 환자를 대상으로 한 APX-115의 2상, 이중 맹검, 위약 대조, 유효성 및 안전성 연구 2) 임상시험 단계 : 2상 임상 시험 3) 대상질환명(적응증) : COVID-19 (코로나바이러스감염증-19) 4) 임상시험 신청(승인)일 및 승인(시험)기관 : - 신청일 : 2020년 12월 31일 - 승인일 : 2021년 03월 24일 - 임상승인기관 : 미국식품의약국(U.S. FDA: U.S. Food and Drug Administration) - 임상시험기관 : 미국내 12개 병원, 필요한 경우 미국외 타 국가에서 진행할수 있음 5) 임상시험 등록번호 : IND154014 6) 임상시험의 목적 : - COVID-19 환자에서, APX-115의 안전성, 유효성, 내약성 및 약동학을 평가 7) 임상시험 시행 방법 : - 임상시험 대상 환자 규모 : 80명 - 실시 기간 : 투약기간 14일 - 실시방법 : 다기관, 무작위 배정, 이중눈가림, 위약대조 8) 기대효과 : - 코로나바이러스 감염질환인 COVID-19 를 위한 항바이러스, 항염증, 항섬유화를 타겟으로 하는 새로운 치료전략으로의 APX-115의 가능성 확인. COVID-19 진단 된 지 14일 이내의 환자들이 포함되어, 긴급사용 승인을 받은 항바이러스제, 항체치료제 보다 넓은 범위의 환자가 선정됨. - APX-115의 COVID-19 에서의 안전정과 유효성을 확인 및 치료제로서의 개발을 위한 2상 임상시험으로, 결과 분석 후 치료적 확증을 위한 임상시험에 진입이 가능하며, 치료적 확증 임상시험 완료 후 긴급사용 승인등의 신속심사 절차 시도 가능. |
|
| 3. 사실발생(확인)일 | 2021-03-24 | |
- 10월경 면역항암제 (APX-NEW) EA계약의 본계약 여부 확인
2020년 10월 체결된 글로벌 제약사와의 EA(Evaluation Agreement) 계약을 바탕으로 오는 10월 실험이 종료될 예정
- 10월경 황반변성 (APX-1004F) 국내 임상1상 테스트
앞서 지난 2018년 삼진제약(005500)에 기술이전(아시아판권)
주사제에서 점안제(특허등록)로 바꿔 지난 2월 국내 임상 신청계획서(IND)를 신청
기존 치료제들은 주사제인데 비해, APX-1004F는 점안제(안약)로 안구 후안부까지 약물이 도달가능한 차별화된 장점이 있어 해당 시장의 게임체인저로서 성장을 기대
기존 황반변성 치료제인 ‘아일리아’와 비교했을 때 치료 효과가 높고, 병용 투여 시 효과 상승을 보임
경쟁약물 대비 제형과 원가경쟁력 측면에서 긍정적인 평가를 얻어 대형 제약사와 약물실사도 진행 중
APX-115와 같은 성분이므로 APX-115의 임상 2상 데이터가 좋을 경우 연말이나 내년 초 기술수출될 가능성 있음
- 연말경 FDA가 희귀의약품 지정한 혈액암 치료제 ‘Apta-16’ 국내 1/2상 투약 시작
Apta-16는 압타머약물접합체(Apta-DC) 플랫폼 기반 난치성암 치료제
혈액암은 다른 암종과 다르게 혈액테스트 결과와 실제 임상 결과가 약 95%가 일치하기 때문에 많은 글로벌 제약사가 현재 회사의 임상 진행 현황을 문의하고 논의중
삼진제약에 기술이전
- 비알콜성 지방간염 치료제 NASH(APX-311)
프랑스에서 임상 1상을 완료하고 최근 미국 등에서 관련 특허를 확보해 글로벌 제약사에 기술이전을 검토 중
해당 물질은 내년 임상 2상에 진입할 전망임. 임상 진행이 종합 병원에서만 가능해 코로나19 장기화 사태로 현재 임상 개시가 지연되고 있음
NASH 환자 수는 지속적으로 증가하고 있지만, 전 세계적으로 아직 정식 허가받은 치료제가 없는 상황.
시장 규모는 2026년 약 30조원에 이를 것으로 추정
- 췌장암 치료제 (Apta-12) 기술 수출 가능성을 염두에두고 물질검증(비임상) 진행중
암세포에 우수한 항암 효능과 부작용 개선(내성 극복) 효과 및 젬시타빈 내성 문제 극복이라는 결과를 확보하여 차세대 표적 항암제로서 경쟁력을 갖추고 있음
미국 호프바이오사이언스에 기술이전
- 2021년 당뇨병성 신증, 혈액암, 면역항암제, 비알콜성지방간염, 황반변성 , 코로나치료제 중 2건 조단위 LO 체결 목표
'국내주식' 카테고리의 다른 글
| [매각관련주] 휴젤 gs에 인수, 다나와 매각 추진설 보도 주가는? (1) | 2021.08.11 |
|---|---|
| [바이오주] k백신 - 셀리드 코로나백신개발 추진, 주가는? (0) | 2021.08.11 |
| 카페24- 네이버(naver) 지분 교환(제3자유상증자) 내용? 주가는? (0) | 2021.08.10 |
| [바이오주] 셀트리온 코로나19 치료제 ct-p59 변경허가 신청 주가는? (0) | 2021.08.10 |
| [리튬관련주] 일진머티리얼즈 공장 투자내용 주가와 사업내용? (0) | 2021.08.10 |




댓글